POLITÍCA NACIONAL
Especialistas apontam falhas na política de preços de medicamentos e defendem mudanças
POLITÍCA NACIONAL

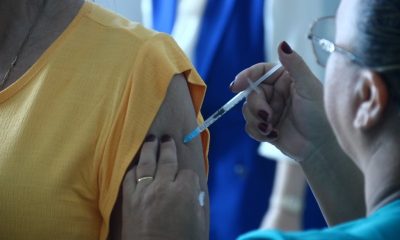
Especialistas ouvidos pela Comissão de Saúde da Câmara dos Deputados nesta quinta-feira (14) defenderam mudanças na política de preços de medicamentos. Durante o debate, eles apontaram diferença entre o preço máximo autorizado pela Câmara de Regulação do Mercado de Medicamentos (CMED) e os valores cobrados nas farmácias.
No Brasil, os preços dos medicamentos são regulados pela CMED e os limites máximos são reajustados anualmente com base em inflação, produtividade, custos de produção e concorrência. As farmácias podem vender os produtos abaixo do teto definido pelo órgão, mas não acima. O modelo de regulação de preços foi criado pela Lei 10.742/03.
A coordenadora de Propriedade Intelectual da Associação Brasileira Interdisciplinar de Aids, Susana Van Der Ploeg, criticou as distorções nos preços de teto da CMED, que estariam muito acima dos praticados no mercado. Ela apresentou dados mostrando que o Brasil paga até 600% a mais por medicamentos contra o HIV em comparação com países vizinhos.
Já Marina Paulelli, do Instituto de Defesa de Consumidores (Idec), apontou que as regras atuais não coíbem aumentos bruscos. Ela também criticou a prática de farmácias que condicionam descontos ao fornecimento do CPF. “Vincular descontos à entrega de dados pessoais é uma prática abusiva e em desacordo com a Lei Geral de Proteção de Dados (LGPD)”, defendeu.
Susana Van Der Ploeg defendeu a aprovação do Projeto de Lei 5591/20, do Senado, que fortalece a capacidade regulatória da CMED e prevê revisão periódica dos tetos de preços.
O autor do requerimento para realização da audiência, deputado Jorge Solla (PT-BA), destacou que a escala de compras do Sistema Único de Saúde (SUS) deve ser utilizada como ferramenta de negociação.
“A escala é definidora do preço. O Brasil é o único país com mais de 100 milhões de habitantes que tem um sistema de saúde público universal”, afirmou o parlamentar.

Indústria farmacêutica
A diretora de Acesso ao Mercado da Associação da Indústria Farmacêutica de Pesquisa (Interfarma), Helaine Capucho, discordou das críticas ao setor.
“Não é a indústria que define o preço que será praticado no país. Em uma cesta internacional de comparação, o Brasil trabalha com o menor preço como referência para venda ao consumidor e ao governo”, disse.
Ela também afirmou que a carga tributária influencia os preços.
“No Brasil, os tributos chegam a 45% do valor de um medicamento”, declarou.
Helaine Capucho defendeu a aprovação de dois projetos:
- PL 2583/20, aprovado pela Câmara e em análise no Senado, cria a Estratégia Nacional de Saúde do Complexo Econômico-Industrial da Saúde. A proposta busca ampliar a autonomia do Brasil na produção de medicamentos, vacinas, insumos e equipamentos para reduzir a dependência externa do SUS; e
- PL 667/21, que permite que o Ministério da Saúde negocie a compra de novos medicamentos quando houver dúvidas sobre custos ou eficácia do tratamento.
SUS e laboratórios públicos
O coordenador-geral de Assistência Farmacêutica e Medicamentos Estratégicos do Ministério da Saúde, Luiz Henrique Costa, explicou que a compra de medicamentos é centralizada pelo ministério em parceria com secretarias estaduais de saúde.
Segundo Costa, mais de 53% das compras são feitas em laboratórios privados, que recebem 61% do orçamento destinado à aquisição de medicamentos. Já os laboratórios públicos respondem por quase 40% do estoque e recebem cerca de 26% do orçamento.
Representantes do Instituto de Tecnologia em Fármacos (Farmanguinhos), vinculado à Fundação Oswaldo Cruz (Fiocruz), também participaram da audiência.
Farmanguinhos é o maior laboratório farmacêutico oficial ligado ao Ministério da Saúde. O instituto produz principalmente medicamentos antirretrovirais, que representam 56% da produção da unidade.
A diretora do instituto, Silvia Pereira Santos, ressaltou que a produção pública atua como reguladora de mercado.
“Onde a produção pública é estratégica, o preço do mercado reduz e o acesso à saúde aumenta”, disse. Ela citou o exemplo do tacrolimo, imunossupressor para transplantes que hoje tem produção 100% nacional, com redução de até 70% no preço.
Modernização das regras
O secretário executivo substituto da CMED, Frederico Mocha, informou que novas regras de precificação entram em vigor no final de maio (Resolução 3/25). A norma amplia de 9 para 14 a lista de países usados como referência para fixar preços no Brasil e busca incentivar a inovação incremental.
Mocha também destacou que a CMED estuda mecanismos para permitir a revisão extraordinária de preços, tanto para cima quanto para baixo, seguindo boas práticas internacionais.
Reportagem – Luiz Cláudio Canuto
Edição – Geórgia Moraes
Fonte: Câmara dos Deputados

POLITÍCA NACIONAL
Comissão aprova o uso de novas assinaturas digitais

A Comissão de Ciência, Tecnologia e Inovação da Câmara dos Deputados aprovou projeto de lei que permite o uso de novas assinaturas eletrônicas para comprovar a autoria de documentos digitais.
Pelo texto, serão aceitas todas as ferramentas para atestar autoria que constem na Lei das Assinaturas Eletrônicas (Lei 14.063/20), inclusive tecnologias que não usem os certificados oficiais do governo (sistema ICP-Brasil).
O colegiado aprovou o substitutivo do relator, deputado Rodrigo da Zaeli (PL-MT), ao PL 1195/25, do deputado Capitão Alberto Neto (PL-AM). O parecer ampliou o alcance do projeto original que se limitava a incluir o uso do blockchain como meio de assinatura oficial. “O projeto permite maior alcance a essa e outras tecnologias, presentes e futuras”, reforçou Zaeli.
Para que o documento tenha validade legal, basta que as duas partes envolvidas concordem com o formato escolhido.
A proposta altera a medida provisória 2200-2/01 que regula as assinaturas digitais no Brasil e cria a Infraestrutura de Chaves Públicas Brasileira (ICP-Brasil).
Esse sistema garante que um documento assinado no computador tenha o mesmo valor legal que um documento assinado no papel. Atualmente, a regra foca em um modelo fechado. Nele, o governo fiscaliza as empresas que vendem certificados digitais para a população.
O texto aprovado permite que sistemas independentes (descentralizados) também sirvam para validar documentos. Com isso, tecnologias modernas como o blockchain passam a ter validade jurídica para assinar arquivos eletrônicos.
Próximos passos
A proposta que tramita em caráter conclusivo será agora analisada pela Comissão de Constituição e Justiça e de Cidadania. Para virar lei, precisa ser aprovada perla Câmara e pelo Senado.
Saiba mais sobre a tramitação de projetos de lei
Reportagem – Emanuelle Brasil
Edição – Ana Chalub
Fonte: Câmara dos Deputados
-

 ESPORTES1 dia atrás
ESPORTES1 dia atrásA Reforma Tributária Pode Destruir o Esporte Brasileiro Fora do Futebol Bilionário
-

 ESPORTES7 dias atrás
ESPORTES7 dias atrásJogo do Flamengo na Colômbia é cancelado após atos de violência da torcida
-

 ESPORTES1 dia atrás
ESPORTES1 dia atrásCÂMARA APROVA PLP 21/2026 E SALVA ESPORTE OLÍMPICO DE SAFARI TRIBUTÁRIO; FLAMENGO E PINHEIROS LIDERARAM ARTICULAÇÃO
-

 POLÍCIA3 dias atrás
POLÍCIA3 dias atrásPolícia Militar prende homem suspeito de agredir namorada em Nova Xavantina
-

 POLÍTICA6 dias atrás
POLÍTICA6 dias atrásDeputado Alex Sandro cobra instalação de passarelas na Avenida da FEB para evitar tragédias e preparar região para o BRT
-

 Sinop6 dias atrás
Sinop6 dias atrásSinop sedia formação regional e firma termo de compromisso para fortalecimento dos direitos dos adolescentes
-

 ESPORTES4 dias atrás
ESPORTES4 dias atrásFlamengo vence o Grêmio fora de casa e segue firme no Brasileirão
-

 POLÍTICA6 dias atrás
POLÍTICA6 dias atrásMato Grosso 278 anos: Assembleia Legislativa fortalece a voz dos municípios